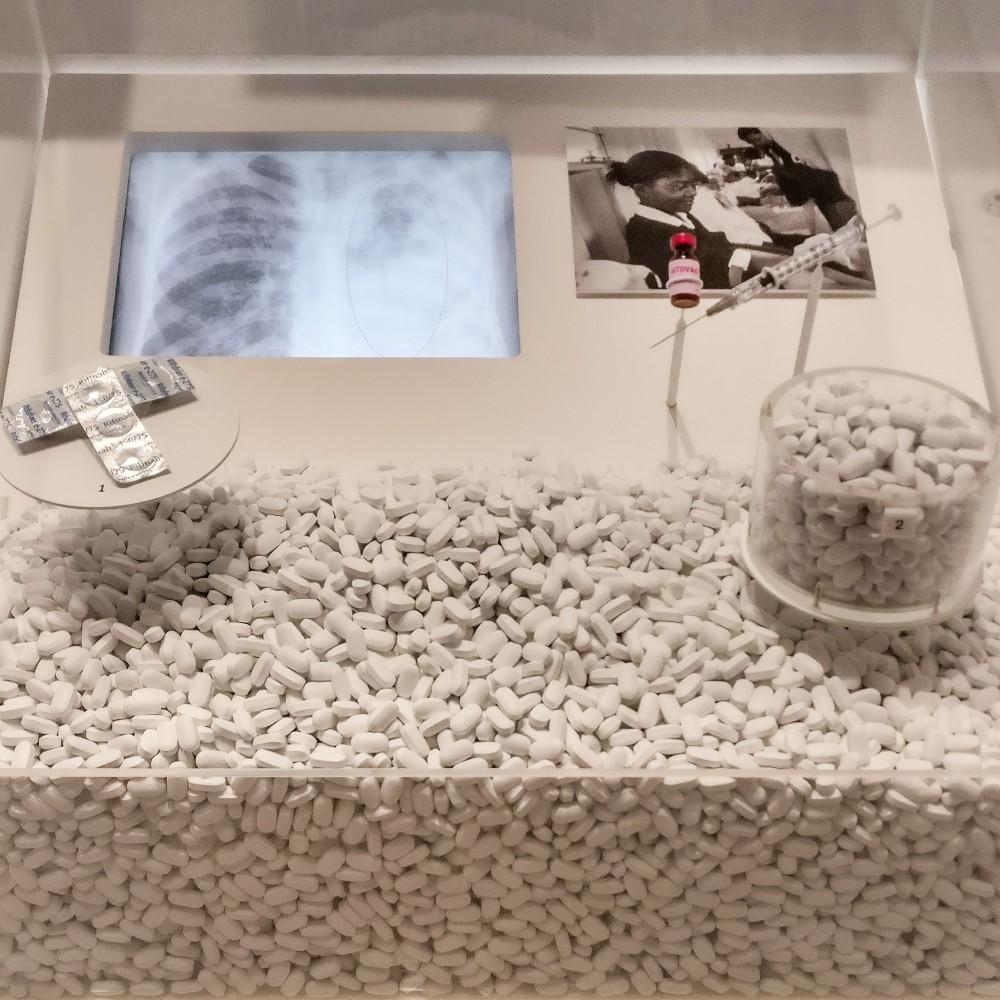
Un proyecto en el que participa el CSIC pretende dar los medicamentos más correctos, mejorar las tasas de curación y ayudar a detener la propagación
Según los datos de la Organización Mundial de la Salud, el año 2016 10,4 millones de personas enfermaron de tuberculosis y 1,7 millones murieron por esta enfermedad
Castellón Información
Investigadores del Instituto de Biomedicina de Valencia (IBV) del Consejo Superior de Investigaciones Científicas (CSIC) han contribuido al CRyPTIC consortium (http://www.crypticproject.org), un proyecto liderado por la Universidad de Oxford que investiga la susceptibilidad de los pacientes de tuberculosis a distintos medicamentos mediante el estudio del ADN de la bacteria. En el trabajo también han participado el Hospital Universitario y Politécnico La Fe y a la Fundación para El fomento de la Investigación Sanitaria y Biomédica de la Comunidad Valenciana (FISABIO).
La tuberculosis es causada por la 'Mycobacterium tuberculosis', una bacteria que casi siempre afecta a los pulmones. Se trata de una afección curable y que se puede prevenir. La Organización Mundial de la Salud (OMS) considera que la tuberculosis es una de las 10 principales causas de mortalidad en el mundo. En 2016, 10,4 millones de personas enfermaron de tuberculosis y 1,7 millones murieron por esta enfermedad. Más del 95% de estas muertes se producen en países en vías de desarrollo.
El investigador del CSIC Iñaki Comas explica que “la OMS recomienda que se hagan pruebas de susceptibilidad a los medicamentos contra la tuberculosis, para tomar mejores decisiones acerca de cómo tratar a los pacientes y así mejorar los resultados. Por eso, se decidió evaluar si la secuenciación del ADN de la bacteria Mycobacterium tuberculosis podría servir para predecir con precisión los perfiles de susceptibilidad a los fármacos antituberculosos de uso más común”.
Los investigadores participantes en el estudio han analizado secuencias de genoma completo de la bacteria Mycobacterium tuberculosis de un total de 10.209 cepas de tuberculosis aisladas de pacientes en 16 países distintos de los seis continentes. El estudio demuestra que los perfiles de resistencia a partir del dato genómico pueden predecir con alta sensibilidad y especificad si un paciente será o no resistente a un fármaco de primera línea. Una de las ventajas de usar la secuenciación genómica para predecir los perfiles de resistencias es que reduce la cantidad de pruebas fenotípicas
que se hacen en los laboratorios para los casos más comunes, y que permite centrarse en el diagnóstico de casos especialmente complejos.
La OMS se propone acabar con la tuberculosis para el año 2035, y esto se conseguirá gracias al desarrollo de mejores técnicas preventivas, diagnósticas y terapéuticas. “Hasta ahora, los altos costos de las pruebas impedían que se realizasen estudios de susceptibilidad a los medicamentos en los países más pobres. Los avances recientes en las técnicas de secuenciación del genoma nos permiten evaluar la susceptibilidad a los medicamentos de manera más rápida, más escalable y probablemente menos costosa que si realizáramos pruebas fenotípicas”, concluye Comas.
Quedan sin embargo obstáculos al uso rutinario de la secuenciación genómica en la práctica clínica. Por una parte, la capacidad de secuenciación genómica en muchos países, y particularmente en aquellos donde más casos se dan, es muy limitada, al igual que la capacidad analítica de los resultados. Además, la secuencia genómica todavía se extrae a partir de ADN de la bacteria en cultivo, que tarda entre dos y tres semanas en crecer; mientras que lo ideal sería hacerlo directamente sobre esputo. En el IBV, junto con otros centros de investigación de todo el mundo, se trabaja en desarrollar protocolos para avanzar en esas direcciones, incluyendo la transferencia de conocimientos y tecnológica a países como México y Mozambique.
Los resultados de este estudio ya han influido en las decisiones tomadas en Inglaterra, los Países Bajos y el Centro de Salud Pública de Wadsworth, en el Estado de Nueva York, dirigidas a reducir la dependencia del cultivo bacteriano en los tratamientos contra la tuberculosis y administrar el tratamiento de acuerdo con los resultados de la secuenciación del ADN. Así se conseguirá dar los medicamentos correctos a más pacientes, mejorarán las tasas de curación y, además, se ayudará a detener la propagación de algunas cepas de tuberculosis resistentes a los medicamentos.